Nacional Dependencias Federales
Lento, el desarrollo de la vacuna Patria contra el Covid-19
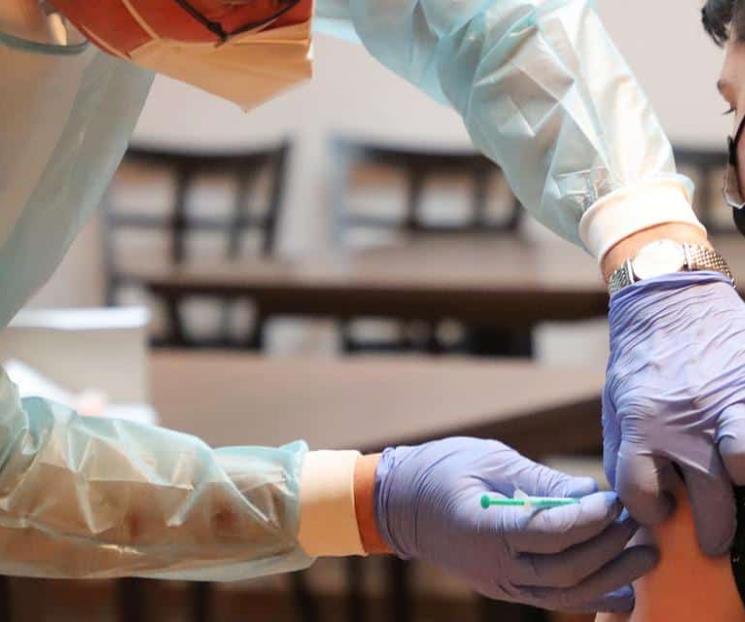
Publicación:28-05-2022
TEMA: #Covid-19 México
El proyecto concentra dos tecnologías que fueron desarrolladas en EU con la intención de satisfacer la demanda a escala mundial de una vacuna contra Covid-19
IUDAD DE MÉXICO/EL UNIVERSAL.- El anuncio del proyecto de la vacuna Patria contra el Covid-19, realizado hace dos años, estaba lleno de buenas intenciones aderezadas con la promesa de una vacuna 100% mexicana que estaría lista para diciembre de 2021. La realidad siempre es más consistente que los buenos deseos. El proyecto concentra dos tecnologías que fueron desarrolladas en EU con la intención de satisfacer la demanda a escala mundial de una vacuna contra Covid-19 a bajo costo y que han servido de plataforma a varios países para intentar gestar una vacuna propia, pero aún sin concretarse alguna. Una de estas tecnologías fue desarrollada por la Universidad de Texas, en Austin. Se trata de una proteína HexaPro, una versión modificada de la proteína espiga del SARS-CoV-2 con seis alteraciones estratégicas en su estructura molecular que producen una proteína más estable y resistente. Por otro lado, el laboratorio Avimex, el elegido por Conacyt para desarrollar el proyecto de Patria, usa la licencia exclusiva de uso de la plataforma rNDV en México para el desarrollo de vacunas contra el Covid-19 de la Escuela Icahn de Medicina en Monte Sinaí (NY). La plataforma rNDV también ha servido como base para el desarrollo de otros proyectos de vacuna contra el virus SARS-CoV-2 en otros países como Brasil, Vietnam y Tailandia. En el caso de Brasil, según informes del Instituto Butantan, se trata de una vacuna con prometedores resultados como una vacuna única contra el Covid-19 y la gripe, pero aún están en la fase de estudios preliminares; los estudios clínicos se realizarían hasta el año siguiente. Las vacunas de Vietnam y Tailandia, COVIVAC y HXP-GPOVac, respectivamente, están culminando su segunda fase, como lo detallan el Institute of Vaccines and Medical Biologicals (IVAC) y el Center for Covid-19 Situation Administration (CCSA).
PASO A PASITO
Después de un proceso que inició en 2020 para la vacuna Patria, se transitó por obtener la licencia de uso, desarrollar y evaluar in vitro a los candidatos vacunales y realizar las pruebas preclínicas en animales. Finalmente, hace aproximadamente un año inició el estudio clínico fase 1. Alrededor de 199 millones de pesos es lo que el gobierno mexicano invirtió hasta finales del 2021 en el proyecto, más la inversión del propio laboratorio. Finalmente se presentaron los resultados de estas primeras pruebas en humanos a mediados de febrero de este año. Los resultados, publicados en el repositorio MedRxiv resumían que el candidato a vacuna basado en un virus de la enfermedad de Newcastle (NDV), recombinante vivo que expresa una versión estable de la proteína espiga en las células infectadas, así como en la superficie de la partícula viral (AVX/COVID-12-HEXAPRO, también conocido como NDV-HXP-S), fue evaluado por vía intramuscular, intranasal o intranasal seguida de vías intramusculares en un ensayo clínico con 91 voluntarios en México. Se subraya que los resultados difundidos corresponden a las pruebas tomadas en todas y todos los voluntarios al día 42 desde la primera inoculación. El objetivo principal del ensayo fue evaluar la seguridad de la vacuna y el objetivo secundario fue determinar la inmunogenicidad de los diferentes regímenes mencionados. Como generalmente sucede en los estudios clínicos en esta primera etapa del desarrollo de una vacuna, el ensayo no fue aleatorizado ni controlado con placebo. El análisis de esta vacuna candidata que se puede cultivar en huevos embrionados, de forma similar a las vacunas contra el virus de la influenza, reportó que era segura y que las dosis más altas probadas eran inmunogénicas cuando se administraban por vía intramuscular o intranasal seguida de una administración intramuscular, lo que proporcionó la base para un mayor desarrollo clínico de la vacuna candidata. Cabe señalar que en la actualidad las vacunas intranasales se han mostrado como una apuesta para prevenir infecciones a largo plazo de Covid 19. Este tipo de biológicos se centran en defender una de las zonas estratégicas del cuerpo para escudarse del virus, como la mucosa de revestimiento de las vías respiratorias, donde el coronavirus inicia su trayectoria en el organismo. Así se busca evitar la reproducción del coronavirus en las vías respiratorias altas. Además de la propuesta mexicana existen otras vacunas que están intentando probar la eficacia de una vacuna contra el SARS-CoV-2 administrada por esta vía, como el Instituto Pasteur en Francia, que mantiene un proyecto de refuerzo nasal a una vacuna intramuscular.
« El Universal »




